 Estudo selecionado como primeiro Late Breaking Abstract do ASH 2022 mostrou resultados de blinatumomabe (blin) no tratamento de pacientes com leucemia linfoblástica aguda (LLA) recém-diagnosticada, em apresentação de Mark R. Litzow (foto), da Mayo Clinic. A adição de blin à quimioterapia de consolidação resultou em benefício clínico e estatisticamente significativo de sobrevida global (HR: 0,42, 95% CI: 0,24 - 0,75; bilateral p=0,003), representando novo padrão de tratamento para pacientes com LLA BCR::ABL1 negativo.
Estudo selecionado como primeiro Late Breaking Abstract do ASH 2022 mostrou resultados de blinatumomabe (blin) no tratamento de pacientes com leucemia linfoblástica aguda (LLA) recém-diagnosticada, em apresentação de Mark R. Litzow (foto), da Mayo Clinic. A adição de blin à quimioterapia de consolidação resultou em benefício clínico e estatisticamente significativo de sobrevida global (HR: 0,42, 95% CI: 0,24 - 0,75; bilateral p=0,003), representando novo padrão de tratamento para pacientes com LLA BCR::ABL1 negativo.
Adultos com leucemia linfoblástica aguda (LLA) recém-diagnosticada podem alcançar alta taxa de remissão completa (CR) com quimioterapia convencional, mas frequentemente recaem e têm taxas de sobrevida abaixo do ideal, mesmo com negatividade da doença residual (DRM) após a indução.
Blinatumomabe (blin) é um anticorpo específico das células T aprovado pela FDA para pacientes com LLA de linhagem B com doença recidivante/refratária ou pacientes em RC morfológica que são MRD positivos (> 0,1%).
Neste estudo randomizado de fase III, realizado por pesquisadores do ECOG-ACRIN Cancer Research Group, foram considerados pacientes para quimioterapia convencional com ou sem blin para determinar se aqueles que se tornaram MRD negativos (<0,01%) após a quimioterapia de indução poderiam ter melhores resultados com a adição do novo agente blinatumomabe.
Foram elegíveis pacientes com LLA de linhagem B entre 30 e 70 anos com BCR::ABL1 negativo, que receberam inicialmente 2,5 meses de quimioterapia de indução combinada utilizando um regime semelhante ao BFM adaptado do ensaio clínico E2993/UKALLXII, com indução de remissão estendida, adição de pegaspargase para pacientes <55 anos de idade e adição de rituximabe para pacientes CD20 positivos (figura 1). Após a indução da remissão (etapa 1), pacientes em remissão morfológica completa (CR/CRi) continuaram no estudo e receberam um curso de intensificação de altas doses de metotrexato com pegaspargase para profilaxia do SNC (etapa 2).
Posteriormente, sua remissão e status de MRD foram determinados centralmente por citometria de fluxo com negatividade de MRD definida como <0,01%. Todos os pacientes foram então randomizados para receber quatro ciclos adicionais de quimioterapia de consolidação ou dois ciclos de blin por 28 dias cada, seguido por 3 ciclos de quimioterapia de consolidação, outro ciclo de 4 semanas de blinatumomabe (3º ciclo de blinatumomabe) e um ciclo adicional de quimioterapia, seguido de um 4º ciclo de blinatumomabe (etapa 3).
Os autores descrevem que os pacientes receberam o mesmo número de ciclos e doses de quimioterapia em cada braço. Após a conclusão da quimioterapia de consolidação +/- blin, os participantes receberam 2,5 anos de terapia de manutenção POMP desde o início do ciclo de intensificação (etapa 4). A realização do transplante alogênico de células hematopoiéticas (HCT) ficou a critério do médico assistente, preferencialmente após os dois primeiros ciclos de blin no braço blin ou a qualquer momento após a quimioterapia de intensificação no braço controle. Após a aprovação da FDA de blin para doença positiva para MRD em março de 2018, pacientes com MRD+ após a intensificação foram designados para o braço blin do estudo e não mais randomizados.
O endpoint primário foi comparar a sobrevida global (SG) em pacientes com MRD que receberam blin + quimioterapia, com a SG dos pacientes que receberam apenas quimioterapia. Com um mínimo de 190 pacientes MRD negativos, o estudo teve poder de 80% para detectar redução de 45% na razão de risco no braço de blinatumomabe em relação ao braço de quimioterapia de controle, usando o teste de log rank unilateral no nível de significância de 0,025 e considerando 2 anos de seguimento. As estimativas de SG foram calculadas usando o método de Kaplan-Meier. A comparação de SG entre os braços de tratamento foi realizada usando o teste estratificado de log-rank e o modelo de riscos proporcionais de Cox com idade, status de CD20, uso de rituximabe e HSCT como fatores de estratificação.
Resultados
Foram selecionados 772 pacientes e 488 foram inscritos na terapia de indução da etapa 1, com idade média de 51 anos (intervalo de 30 a 70). Os autores descrevem que 224 pacientes MRD negativos foram randomizados (n= 112 em cada braço). Dessa população, 22 pacientes (pts) em cada braço procederam ao transplante alogênico. A taxa CR/CRi após a quimioterapia de indução foi de 81%. Entre os pts MRD negativos, na terceira análise interina de eficácia, 56 pts morreram, 17 no braço cego e 39 no braço de quimioterapia de controle.
Os resultados apresentados no ASH 2022 mostram que o limite superior para análise de eficácia foi ultrapassado em favor de blinatumomabe, com benefício significativo na sobrevida global em favor do braço de blin (SG mediana não alcançada vs. 71,4 meses; razão de risco 0,42, 95% CI: 0,24 - 0,75; bilateral p=0,003). O seguimento mediano foi de 43 meses.
“A adição de blin à quimioterapia de consolidação resultou em sobrevida global significativamente melhor em pacientes com LLA de linhagem B recém-diagnosticada que eram MRD negativos após a quimioterapia de intensificação. Não foram observadas preocupações significativas de segurança. A adição de blin à quimioterapia de consolidação em pacientes adultos com idades entre 30 e 70 anos representa um novo padrão de tratamento para pacientes com LLA negativa BCR::ABL1”, concluem os autores.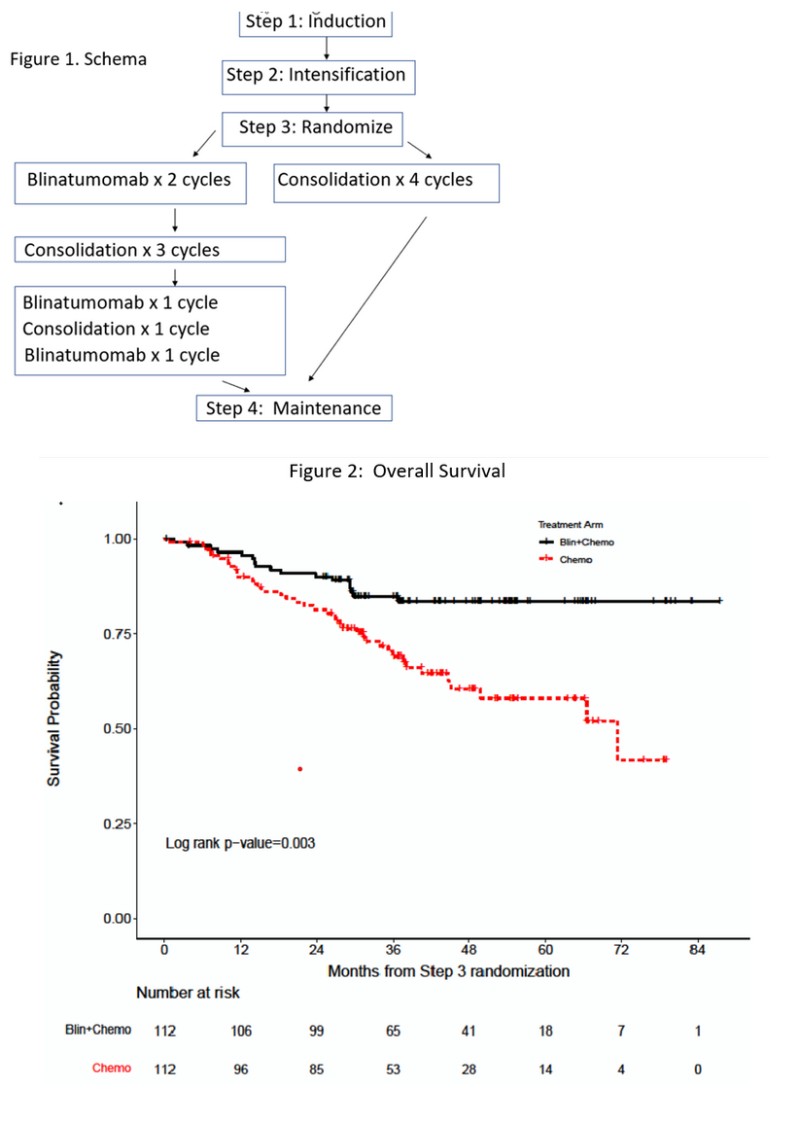 Referência: LBA-1 Consolidation Therapy with Blinatumomab Improves Overall Survival in Newly Diagnosed Adult Patients with B-Lineage Acute Lymphoblastic Leukemia in Measurable Residual Disease Negative Remission: Results from the ECOG-ACRIN E1910 Randomized Phase III National Cooperative Clinical Trials Network Trial
Referência: LBA-1 Consolidation Therapy with Blinatumomab Improves Overall Survival in Newly Diagnosed Adult Patients with B-Lineage Acute Lymphoblastic Leukemia in Measurable Residual Disease Negative Remission: Results from the ECOG-ACRIN E1910 Randomized Phase III National Cooperative Clinical Trials Network Trial
Program: General Sessions
Session: Late-Breaking Abstracts Session
Tuesday, December 13, 2022, 9:00 AM-10:30 AM
Mark R. Litzow, MD et al








