Anvisa aprova indicação de durvalumabe perioperatório no câncer de pulmão ressecável
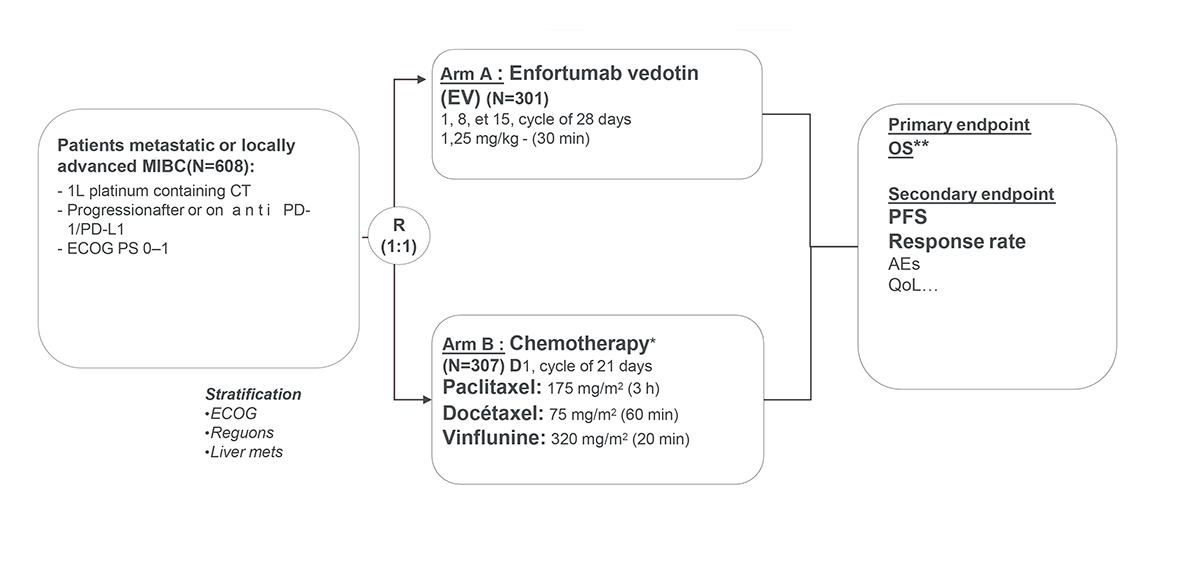
A Agência Nacional de Vigilância Sanitária (ANVISA) ampliou a indicação terapêutica de durvalumabe (IMFINZI®, AstraZeneca) no câncer de pulmão de células não pequenas (CPCNP). A decisão foi publicada no Diário Oficial da União1 (DOU) de 1º de setembro1 com base nas evidências de eficácia e segurança do estudo AEGEAN, que demonstrou benefício de durvalumabe nos desfechos de pacientes com CPCNP no contexto do tratamento com intenção curativa.
O câncer de pulmão é a principal causa de morte por câncer entre homens e mulheres, responsável por cerca de um quinto de todas as mortes por câncer5. A cirurgia se mantém como espinha dorsal do tratamento de intenção curativa para pacientes com CPCNP com doença estadio I-IIIA, como recomendam as diretrizes do NCCN6. No entanto, existem claras necessidades não atendidas mesmo após a ressecção curativa, uma vez que micro metástases podem levar à recorrência da doença7. As taxas de sobrevida global em 5 anos são de 53% para pacientes com estadio IIB e caem para apenas 26% na doença avançada (estádio IIIB)8, 9, 10.