 André Márcio Murad (foto), Coordenador da Disciplina de Oncologia da Faculdade de Medicina da UFMG e Diretor da Clínica Personal Oncologia, apresentou no Rio de Janeiro um overview sobre o tratamento da doença avançada.
André Márcio Murad (foto), Coordenador da Disciplina de Oncologia da Faculdade de Medicina da UFMG e Diretor da Clínica Personal Oncologia, apresentou no Rio de Janeiro um overview sobre o tratamento da doença avançada.
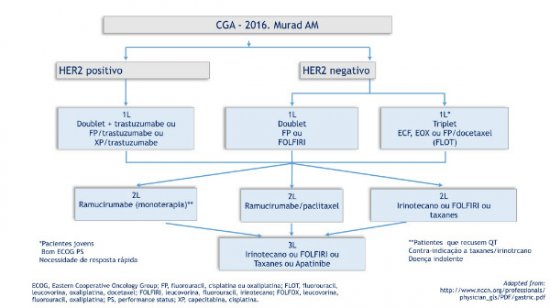
{jathumbnail off}Tratamento de primeira linha
O câncer gástrico avançado (CGA) foi considerado durante muitos anos como um tumor resistente ao tratamento quimioterápico. Nosso grupo, pela primeira vez na literatura, demonstrou a superioridade de um regime quimioterápico em comparação ao melhor tratamento de suporte clínico em 1993 (Murad et al, Cancer. 1993 Jul 1;72(1):37-41). O regime utilizado foi o FAMTX (5-fluorouracil- 5FU-, doxorrubicina, leucovorina e metotrexato), o qual produziu uma sobrevida mediana de 9 meses versus apenas 3 meses para o tratamento de suporte. Estes dados foram posteriormente reproduzidos por mais 2 outros estudos randomizados, e compilados em uma metanálise publicada por Wagner et al (J Clin Oncol. 2006 Jun 20;24(18):2903-9) que incluiu 184 pacientes, estabelecendo-se assim de forma definitiva o benefício da poliquimioterapia no tratamento do CGA, com uma razão de chances de 0,39 (IC:95%; 0,28- 0,52) em relação a sobrevida global, a favor da quimioterapia.
Posteriormente, um estudo publicado por Webb et al (J Clin Oncol. 1997 Jan;15(1):261-7) demonstrou superioridade do regime ECF (epirrubucina, cisplatina e 5FU em infusão contínua de 21 dias) versus o regime FAMTX em termos de mediana de sobrevida: 8,9 meses versus 5,7 meses. Entretanto, mesmo com a incorporação de novos agentes a partir dos anos 2000, como os taxanos, a capecitabina e a oxaliplatina, os avanços obtidos com o emprego da quimioterapia convencional foram bastante modestos, sem êxito em elevar a sobrevida mediana além da barreira dos 12 meses.
Van Cutsem et al (J Clin Oncol 2006, 24:4991-4997) acrescentaram o docetaxel à combinação de cisplatina e 5FU e demonstraram um benefício na sobrevida global mediana (9,2 versus 8,6 meses) com o emprego do regime DCF, entretanto às custas de uma toxicidade acentuada: estomatite graus OMS 3/4 de 21% a 27%, neutropenia febril de 27% a 29% e morte por toxicidade do tratamento da ordem de 5%, o que tornou o regime muito pouco utilizável fora do escopo experimental, pelo menos nas doses propostas pelo estudo original.
Cunningham, et al (N Engl J Med 2008; 358(1): 36-46) publicaram os dados de um estudo fase III (REAL-2) com 1002 pacientes randomizados em quatro braços em formato 2X2, tendo o ECF como braço de referência, e avaliando a não inferioridade da substituição do 5FU pela capecitabina e da cisplatina pela oxaliplatina. A capecitabina não foi inferior ao 5FU (razão de chances: 0,86; IC:95%, 0,80-0,99) e a oxaliplatina não foi inferior à cisplatina (razão de chances: 0,92; IC: 95%, 0,80-1,10). O grupo que recebeu o regime EOX (epirrubicina/oxaliplatina/capecitabina) apresentou maior sobrevida em um ano (46,8% vs 37,7%, p=0,02) e sobrevida global (11,2 vs 9,9 meses, p=0,02) quando comparado ao ECF. Os quatro regimes apresentaram taxas de resposta semelhantes, sem diferença estatística significativa, com 47,9% para EOX, 46,4% para EOF (epirrubicina, oxaliplatina e 5FU), 42,4% para ECX (epirrubicina, cisplatina e capecitabina) e 40,7% para ECF. Os regimes contendo oxaliplatina foram bem tolerados, apresentando menor incidência de neutropenia severa, alopecia e nefrotoxicidade, mas com maiores taxas de neuropatia periférica e diarreia. Embora os regimes ECF e EOX sejam hoje de grande preferência no tratamento do CGA, há dúvidas se a incorporação de uma terceira droga, no caso a epirrubicina, realmente acrescenta benefício.
Um regime apenas com a combinação de 5FU, leucovorina e oxaliplatina (FLO) produziu eficácia superior ao regime FLP (cisplatina/5FU e leucovorina) quando analisados pacientes acima de 65 anos (n=94), em um total de 220 pacientes com CGA (J Clin Oncol 2008; 26(9): 1435-42). O regime FLO revelou-se significativamente superior em relação à taxa de resposta (41,3 versus 16,7%; p=0,012), tempo para falha do tratamento (5,4 versus 2,3 meses; P<0,001), e SLP (6,0 versus 3,1 meses; p=0,029), além de um aumento da sobrevida global (13,9 versus 7,2 meses). Este grupo também apresentou menor toxicidade quanto à leucopenia graus 1-4, náusea, fadiga e nefrotoxicidade, porém maior incidência de neuropatia periférica.
O esquema FOLFIRI (5FU, leucovorina e irinotecano) é igualmente efetivo como regime de primeira linha no tratamento do CGA, tendo sido comparado ao regime ECX (epirrubicina, cisplatina e capecitabina) em um estudo de fase III, apresentando taxas de resposta e sobrevida semelhantes (J Clin Oncol.2014 Nov 1;32(31):3520-6).
Uso de terapia biológica na primeira linha
A incidência da hiperexpressão de HER-2/neu no câncer gástrico apresenta relatos conflitantes. Recente análise sistemática de revisão da literatura para determinação de prevalência da positividade da hiperexpressão por imuno-histoquímica (IHQ) do HER-2 no tumor gástrico revelou grande amplitude de resultados de 4,4 a 53,4%; assim como também a correlação prognóstica é ainda controversa. A incidência de positividade para HER-2 é maior nos tumores do subtipo intestinal de Lauren.
Um estudo de fase III com 594 pacientes reportou prevalência de 15% a 20% de positividade para HER-2 no câncer esôfagogástrico e um aumento de sobrevida global com a associação de quimioterapia convencional (combinação de cisplatina e fluoropirimidina) ao bloqueio de HER-2 com trastuzumabe (anticorpo monoclonal anti HER-2). Este estudo, o ToGA (Trastuzumab for Gastric Cancer), atingiu seu objetivo primário com uma razão de chances de 0,76; ou seja, uma redução do risco de morte de 24% (p=0,004) - (BANG et al, Lancet. 2010 Aug 28;376(9742):687-97). O ensaio demonstrou um ganho de 2,7 meses na sobrevida global (13,8 meses vs. 11,1 meses) e perfil de toxicidade aceitável. Portanto, a adição de um agente biológico à quimioterapia convencional para o CGA fez pela primeira vez com que a barreira dos 12 meses de sobrevida mediana fosse ultrapassada. Uma análise de subgrupos demonstrou inclusive um ganho maior de sobrevida para pacientes com IHQ positiva 2+ e FISH + ou com IHQ 3+, os quais alcançaram uma sobrevida mediana de 16 meses. Apesar do entusiasmo inicial com o desempenho do trastuzumabe no tratamento do CGA, outros agentes alvo-moleculares foram testados em primeira linha em combinação com quimioterapia em estudos de fase III, mas os resultados foram consistentemente negativos: bevacizumabe (anti-VEGF), lapatinibe (anti-Her2), cetuximabe e panitumumabe (anti-EGFR) e rilotumumabe e onartuzumabe (anti-c-MET).
Aflibercepte, um outro antiangiogênico anti-VEGF também foi testado em um estudo randomizado de fase II que também foi negativo. Os sucessivos fracassos destes agentes alvo-moleculares associados à quimioterapia podem ser justificados pela heterogeneidade tumoral inter e intra-pacientes, inclusive em diferentes localizações das metástases, as quais apresentam co-amplificaçōes, co-expressōes e mesmo diferentes mutaçōes em um mesmo paciente, e também por falha na seleção de pacientes, na medida em que os alvos moleculares podem estar sendo avaliados de forma equivocada. Novos desenhos de estudos clínicos baseados no emprego do sequenciamento genético de nova geração (SNG), inclusive com o emprego do DNA livre circulante em sangue periférico (biópsia líquida) como orientação para os possíveis alvos moleculares certamente obterão resultados mais positivos e robustos no futuro. Estes estudos são conhecidos como do tipo "umbrella" e "basket".
Tratamento de segunda linha. Linhas subsequentes
O emprego em segunda linha de quimioterápicos em monoterapia como docetaxel e irinotecano oferece um discreto ganho na sobrevida global para pacientes que progridem à primeira linha. A sobrevida mediana varia entre 4 a 6,5 meses em 3 estudos que compararam estas drogas com o tratamento clínico de suporte. Um estudo subsequente demonstrou equivalência entre o uso de irinotecano e paclitaxel. Uma metanálise dos 3 estudos confirmou o benefício de qualquer uma destas 3 drogas, com uma razão de chances de 0,64 (0,52-0,79), ou seja, uma redução de mortalidade da ordem de 36% (Kim et al. Ann Oncol. 2013 Nov;24(11):2850-4).
Uso de terapia biológica na segunda linha
Agentes alvo-moleculares testados em estudos randomizados como o TDM-1 (anti-Her-2), o everolimo (anti-TOR), o nimotuzumabe (anti-EGFR) e o olaparibe (inibidor de PARP) apresentaram resultados negativos. O ramucirumabe, um anticorpo monoclonal humano IgG1 antagonista do receptor-2 de VEGF, apresentou benefício tanto em monoterapia como em combinação com o paclitaxel na segunda linha. O estudo internacional, randomizado, multicêntrico, placebo-controlado de fase III REGARD (FUCHS et al.Lancet. 2014 Jan 4;383(9911):31-9) comparou ramucirumabe com placebo em segunda linha de tratamento após quimioterapia de primeira linha baseada em platina e fluopirimidina e demonstrou um ganho significativo de sobrevida global mediana de 1,4 mês em comparação ao placebo mais cuidados paliativos exclusivos, além de boa tolerabilidade e maior tempo para deterioração do PS (desempenho clínico).
No mesmo ano, outro estudo de fase III, o RAIMBOW (WILKE et al. Lancet Oncol. 2014 Oct;15(11):1224-35), randomizou 665 pacientes com CGA que já haviam recebido quimioterapia de primeira linha com um composto platínico associado a uma fluoropirimidina para receberem paclitaxel mais placebo versus paclitaxel associado ao ramucirumabe. A combinação com o ramucirumabe demonstrou benefício na sobrevida global mediana sobre placebo e paclitaxel (9,6 meses [95% CI 8,5–10,8] vs 7,4 meses). Houve também um incremento estatisticamente significativo na sobrevida livre de progressão e na taxa de respostas objetivas. Os dois estudos demostraram toxicidades manejáveis e compatíveis com o emprego de um antiangiogênico.
Em um estudo asiático de fase III, outro antiangiogênico inibidor de multiquinase oral, o apatinibe, apresentou resultados positivos em termos de incremento da sobrevida global de pacientes com CGA como terceira linha de tratamento. Entretanto, esta droga, embora promissora, ainda não se encontra disponível em países do ocidente.
Imunoterapia de segunda geração
Outra promessa recente para o tratamento do CGA é a imunoterapia com bloqueio de PD-L1 (programmed death-ligand 1), uma proteína transmembrana com função inibitória da proliferação dos linfócitos T CD8+. O estudo de fase II KEYNOTE-012 avaliou 162 pacientes com câncer gástrico ou da junção esôfago-gástrica recidivado ou metastático quanto à expressão PD-L1, com 40% dos pacientes expressando positividade com pelo menos 1% na IHQ. Para estes, foi administrado o pembrolizumabe (anticorpo monoclonal bloqueador de PD-L1) (Muro et al. Lancet Oncol. 2016 Jun;17(6):717-26). Os resultados sugeriram preliminarmente um benefício com o uso da droga, com taxa de respostas objetivas da ordem de 30% e, com uma duração de seguimento de 8,8 meses, com 33% dos pacientes ainda permanecendo em terapia. A toxicidade foi manejável.
Perspectivas futuras
Por fim, além da melhor seleção das terapias alvo-moleculares e imunoterápicas, vale a pena ressaltar que os resultados preliminares de um estudo randomizado de fase II empregando um novo anticorpo monoclonal anti-claudina 18.2 (o IMAB 362), proteína presente especialmente nas células do câncer gástrico, foram promissores e apresentados em sessão oral do congresso da ASCO-2016. Estima-se que pelo menos 40% dos pacientes com CGA expressem esta proteína em seus tumores. A combinação EOX/IMAB 362 apresentou ganho significativo na sobrevida global de pacientes portadores de CGA em comparação ao emprego de EOX. Os resultados confirmatórios do estudo de fase III estão sendo ansiosamente aguardados.
Autor: André Márcio Murad é Professor Adjunto-Doutor, pesquisador e coordenador da Disciplina de Oncologia da Faculdade de Medicina da Universidade Federal de Minas Gerais (UFMG) e Diretor Clínico da Personal - Oncologia de Precisão e Personalizada.




