 A biópsia líquida tem papel prognóstico no câncer colorretal e potencial para orientar o tratamento. É o que mostram os resultados do estudo IDEA-FRANCE apresentado no Congresso ESMO 2019. O ctDNA plasmático pós-cirúrgico foi capaz de prever a recidiva de metástases em mediana de 10 meses antes da recorrência ser visível em exames radiológicos (taxa de risco 11.33; p = 0.0001), abrindo uma nova perspectiva para a oncologia de precisão em pacientes com câncer colorretal localizado.
A biópsia líquida tem papel prognóstico no câncer colorretal e potencial para orientar o tratamento. É o que mostram os resultados do estudo IDEA-FRANCE apresentado no Congresso ESMO 2019. O ctDNA plasmático pós-cirúrgico foi capaz de prever a recidiva de metástases em mediana de 10 meses antes da recorrência ser visível em exames radiológicos (taxa de risco 11.33; p = 0.0001), abrindo uma nova perspectiva para a oncologia de precisão em pacientes com câncer colorretal localizado.
Este estudo prospectivo considerou 805 pacientes que realizaram biópsia líquida antes da quimioterapia adjuvante para câncer colorretal, entre os 1345/2010 pacientes inscritos na pesquisa IDEA. Mais PS 0 (77% vs 71%) e mais T4 e / ou N2 (28% vs 23%) foram observados nesses 805 pacientes. Desse universo, 109 pacientes (13,5%), possuíam DNA tumoral circulante no sangue. Nesse grupo CtDNA positivo (ctDNA+), a sobrevida livre de doença (SLD) em dois anos foi de 64%, em comparação com 82% naqueles que eram ctDNA negativos (HR: 1,75 (IC 95% 1,25-2,45) p = 0,001). Em análises multivariadas, incluindo idade, gênero, MSI, perfuração, estágio T, estágio N e braço de tratamento, o ctDNA foi confirmado como um marcador prognóstico independente (adj.HR: 1,85 (IC 95% 1,31 a 2,61) p <0,001).
O tratamento adjuvante por 6 meses foi superior a 3 meses tanto em pacientes ctDNA– (HR: 0,69 (IC 95% 0,52 a 0,93) p = 0,015) quanto em pacientes ctDNA+ (HR: 0,50 (IC 95% 0,27 a 0,95) p = 0,033). Curiosamente, em pacientes ctDNA + tratados por 6 meses, o prognóstico foi semelhante ao grupo de pacientes ctDNA- tratado por 3 meses (Figura 1). Em 90% dos casos a terapia adjuvante foi FOLFOX (ácido folínico, fluorouracil e oxaliplatina).
“Neste grande estudo prospectivo, confirmamos que o ctDNA é um fator prognóstico independente no câncer colorretal e que aproximadamente seis em cada 10 pacientes que são ctDNA+ permanecerão livres da doença dois anos após a quimioterapia adjuvante padrão, em comparação com oito em cada dez pacientes com ctDNA negativo”, disse o autor do estudo, Julien Taieb, do Hôpital European Georges Pompidou, em Paris, França. “Agora sabemos que o ctDNA é um fator prognóstico importante para identificar doença residual mínima e será muito útil na estratificação de pacientes em risco de recorrência e na condução de ensaios futuros”, disse Taieb. “Em todos os subgrupos, pacientes com ctDNA + que tiveram apenas três meses de terapia adjuvante tiveram o pior prognóstico”, acrescentou.
Para Alberto Bardelli, da Universidade de Turim, Itália, os resultados abrem novas perspectivas no tratamento do câncer colorretal. “Quando os pacientes são submetidos à cirurgia para um tumor inicial, permanecem dúvidas se a doença foi completamente erradicada e, como resultado, os pacientes geralmente recebem quimioterapia adjuvante. No entanto, diante dos resultados do IDEA-FRANÇA, agora podemos usar um exame de sangue para dizer se o paciente está livre de doença ou não”, analisou. “O estudo também é um dos primeiros a mostrar que em futuro próximo será possível usar a biópsia líquida para direcionar a terapia e identificar quais pacientes podem ser poupados de quimioterapia após a cirurgia. Se novos estudos confirmarem esses resultados, mudarão a prática clínica, indicando que os novos dados são muito empolgantes”, concluiu Bardelli (Clinical trial identification: NCT00958737).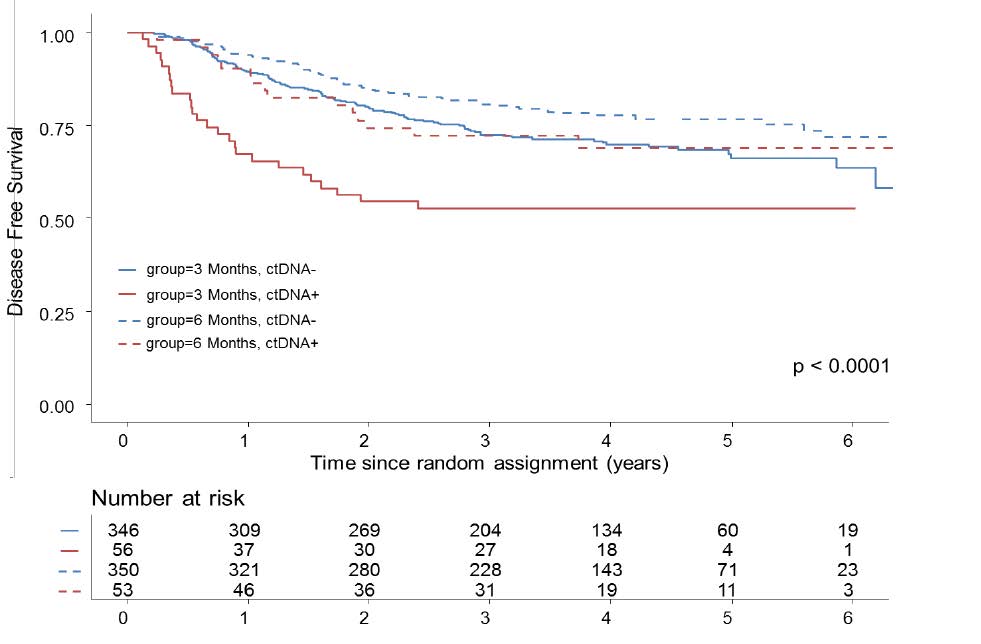
Figura 1. Sobrevida livre de doença de acordo com o status do ctDNA
Referências:
LBA30_PR ‘Analysis of Circulating tumour SNA (ctDNA) from patients enrolled in the IDEA-FRANCE Phase III trial: prognostic and predictive value for adjuvant treatment duration’, Annals of Oncology, Volume 30, Supplement 5, October 2019
Abstract 522O ‘Mutation tracking in circulating tumor DNA (ctDNA) detects minimal residual disease (MRD) in patients with localized colorectal cancer (CRC) and identifies those at high risk of recurrence regardless of stage, lack of CDX2 expression and CMS subtype’, Annals of Oncology, Volume 30, Supplement 5, October 2019
Palavras-chave: ‘Congresso ESMO 2019’, ‘ESMO 2019’, ‘ biópsia líquida’, ‘câncer colorretal’, ctDNA, ‘IDEA-FRANÇA’, ctDNA, ‘doença residual mínima’, ‘risco de recorrência’




