 Estudo internacional randomizado de fase III (MATRIx) que compara HDC-ASCT com terapia de consolidação não mieloablativa em pacientes com linfoma primário do sistema nervoso central (PCNSL) recém-diagnosticados apresentou no ASH`22 a primeira análise envolvendo o endpoint primário de sobrevida livre de progressão (SLP). Selecionado entre os Late Breaking Abstracts da edição deste ano, o estudo demonstra que a consolidação com HDC-ASCT apresenta resultados significativamente melhores de SLP do que a quimioimunoterapia não mieloablativa, com excelente relação risco-benefício (LBA3). Gerald Illerhaus (foto), do Klinikum Stuttgart, Alemanha, é o principal autor do trabalho.
Estudo internacional randomizado de fase III (MATRIx) que compara HDC-ASCT com terapia de consolidação não mieloablativa em pacientes com linfoma primário do sistema nervoso central (PCNSL) recém-diagnosticados apresentou no ASH`22 a primeira análise envolvendo o endpoint primário de sobrevida livre de progressão (SLP). Selecionado entre os Late Breaking Abstracts da edição deste ano, o estudo demonstra que a consolidação com HDC-ASCT apresenta resultados significativamente melhores de SLP do que a quimioimunoterapia não mieloablativa, com excelente relação risco-benefício (LBA3). Gerald Illerhaus (foto), do Klinikum Stuttgart, Alemanha, é o principal autor do trabalho.
Atualmente, pacientes com linfoma primário do sistema nervoso central (PCNSL) elegíveis para abordagens de tratamento intensivo são tratados com imunoquimioterapia de indução baseada em metotrexato em altas doses (HD-MTX), seguida de consolidação com quimioterapia de altas doses e transplante (HDC-ASCT).
No entanto, não está claro se superar a quimiorresistência e subsequentemente eliminar a doença residual mínima também pode ser alcançado por imunoquimioterapia não mieloablativa de dose convencional, compreendendo agentes citotóxicos não resistentes, capazes de atravessar a barreira hematoencefálica
Este estudo aberto, randomizado, de fase III, envolveu a participação de 56 centros em 5 países (Alemanha, Itália, Dinamarca, Noruega, Suíça). Os principais critérios de elegibilidade foram PCNSL recém-diagnosticado, HIV negativo, idade de 18 a 65 anos independentemente de ECOG PS, ou 66 a 70 anos com ECOG PS ≤ 2 e capacidade funcional adequada.
A indução consistiu em 4 ciclos do regime MATRix (rituximabe 375 mg/m2/d dias 0 e 5; metotrexato 3,5 g/m2 dia 1; citarabina 2 × 2 g/m2/d dias 2 e 3; tiotepa 30 mg/m2 dia 4, a cada 21 dias). A coleta de células-tronco foi realizada após o 2º ciclo. Os pacientes que atingiram pelo menos uma resposta parcial (RP) após a indução foram randomizados para qualquer braço A com dois cursos de regime R-DeVIC (375 mg/m2 dia 0; dexametasona 40 mg/dia dias 1 a 3; etoposide 100 mg/dia m2/d dias 1 a 3; ifosfamida 1500 mg/m2/d dias 1 a 3; carboplatina 300 mg/m2 dia 1); ou braço B, consistindo em HDC com BCNU 400 mg/m2 (dia 6) e tiotepa 2 x 5 mg/kg/d dias 5 e -4) seguido de ASCT.
O endpoint primário de SLP em 3 anos foi analisado por modelo de riscos proporcionais de Cox.
Resultados
Entre julho de 2014 e agosto de 2019, foram inscritos 368 pacientes, com mediana de 59 anos (faixa de 21 a 70), 22,3% acima de 65 anos. Desse total, 346 iniciaram o tratamento, 260 (75%) completaram a terapia de indução e 115 e 114 participantes foram randomizados para os braços A e B, respectivamente. As principais razões para não alcançar a randomização foram toxicidades (n= 87; 25%) e progressão da doença (n= 36; 10%).
Em um seguimento mediano de 44 meses (intervalo 0,2-86), 239 de 346 (69%) pacientes responderam ao tratamento de indução, 27% atingiram remissão completa (CR) e 52% remissão parcial (PR).
Em relação ao perfil de segurança, ambas as estratégias de consolidação foram bem toleradas: R-DeVIC e HDC-ASCT foram concluídas em 100 (87%) e 111 (97%) pacientes, respectivamente. 13 (3,8%) pacientes morreram de complicações relacionadas ao tratamento durante a indução, 11 deles devido a complicações infecciosas neutropênicas.
Os autores descrevem que o tratamento de consolidação com R-DEVIC ou HDC-ASCT resultou em aumento substancial de pacientes com CR (65% no braço A e 68% no braço B, respectivamente; p= 0,71). Os dados apresentados no ASH`22 mostram 79 eventos de SLP: 67 participantes apresentaram doença progressiva após a randomização (47 no braço A e 20 no braço B). Seis pacientes morreram de toxicidade durante o tratamento de consolidação (2 braço A e 4 braço B), e 6 morreram de causas não relacionadas, sem recaída (5 braço A e 1 braço B).
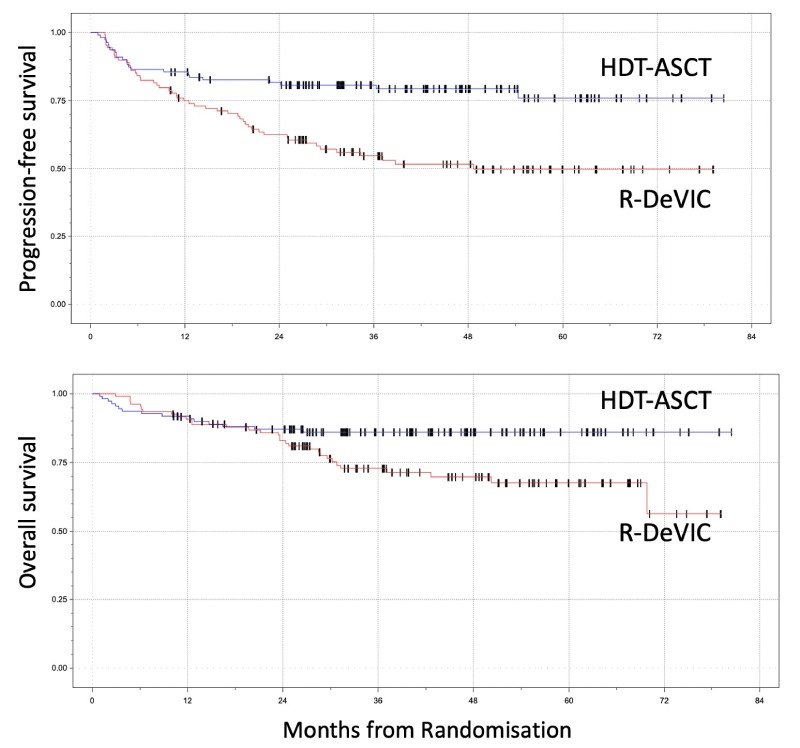
A SLP em 3 anos diferiu significativamente entre os dois braços: 79% (IC 95% 71-86) após HDC-ASCT e 53% (IC 95% 43-62%) após R-DeVIC (HR 0,42; p=0,0003). A sobrevida global (SG) em 3 anos foi de 86% (95% CI 78-91) para o braço HDC-ASCT e 71% (95% CI 61-78) para o braço R-DeVIC (HR 0,47; p=0,01).
A avaliação das funções neurocognitivas não mostrou diferença entre os braços de análise.
“Este estudo randomizado internacional de fase III demonstra que a consolidação com HDC-ASCT resulta em resultados significativamente melhores do que a quimioimunoterapia não mieloablativa. Isso ocorre sem qualquer efeito negativo mensurável nas funções neurocognitivas e com excelente relação risco-benefício”, concluem os autores. “HDC-ASCT é a terapia de consolidação padrão para pacientes com PCNSL aptos”, destacam.
(Estudo MATRIx/IELSG43, NCT02531841).
Referência: LBA-3 Effects on Survival of Non-Myeloablative Chemoimmunotherapy Compared to High-Dose Chemotherapy Followed By Autologous Stem Cell Transplantation (HDC-ASCT) As Consolidation Therapy in Patients with Primary CNS Lymphoma - Results of an International Randomized Phase III Trial (MATRix/IELSG43)
Program: General Sessions
Session: Late-Breaking Abstracts Session
Tuesday, December 13, 2022, 9:00 AM-10:30 AM
Gerald Illerhaus et al.




