Em mais um tópico da coluna ‘Drops de Genômica’, o oncologista Andre Murad (foto) discute os efeitos imunomodulatórios do oncogene KRAS e seu futuro potencial terapêutico. Confira.
Em mais um tópico da coluna ‘Drops de Genômica’, o oncologista Andre Murad (foto) discute os efeitos imunomodulatórios do oncogene KRAS e seu futuro potencial terapêutico. Confira.
Por André Marcio Murad*
As mutações oncogênicas do KRAS são as mais frequentes no câncer humano. O papel das mutações RAS como contribuintes para vários cânceres humanos tornou-se evidente e os mecanismos subjacentes e os reguladores moleculares foram ainda mais elucidados. As proteínas RAS são pequenas GTPases, que atuam como interruptores binários moleculares, onde levam à ativação de várias vias de sinalização como a proteína quinase ativada por mitógeno (MAPK), fosfoinositídeo 3-quinase (PI3K) e RAL-GEF, promovendo uma variedade de processos celulares cruciais, como proliferação, diferenciação e sobrevivência celular em resposta a estímulos extracelulares.
Os membros da família RAS são codificados pelos genes altamente homólogos HRAS, NRAS, KRAS4A e KRAS4B, e suas mutações ativadoras são encontradas em aproximadamente 25% de todos os cânceres humanos. Embora a proliferação sustentada causada pela sinalização oncogênica de KRAS a jusante seja o principal fator de carcinogênese, há evidências crescentes de que ela também medeia efeitos autócrinos e crosstalk com o microambiente tumoral (TME).
Estudos mais recentes conectam mutações KRAS com inflamação promotora de tumor e modulação imune causada por KRAS que leva ao escape imune no TME. Tornou-se mais evidente que as mutações oncogênicas do KRAS medeiam efeitos autócrinos e crosstalk com o TME, particularmente promovendo inflamação e evasão da resposta imune e, finalmente, levando à progressão, invasão e progressão tumoral.
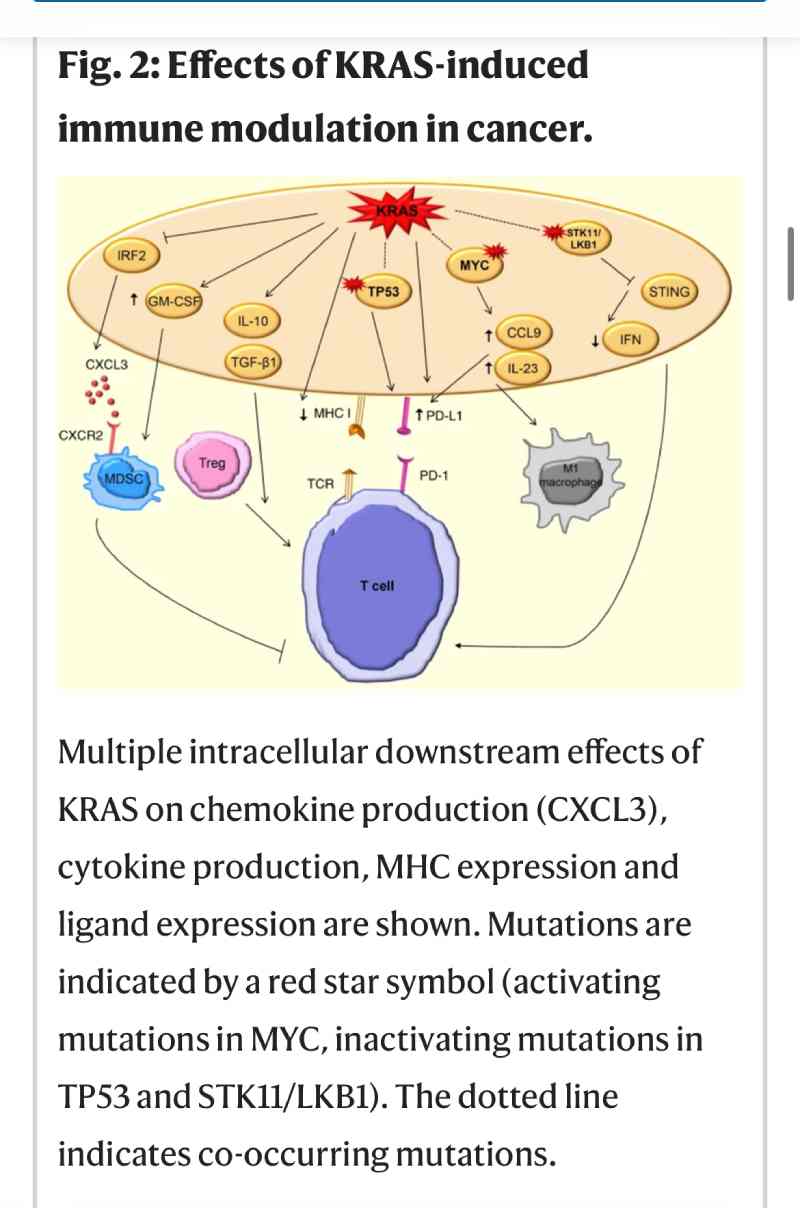
Para exercer esses efeitos, o KRAS oncogênico expresso nas células tumorais remodela as células do estroma circundante por meio da indução de diversas moléculas como citocinas, quimiocinas e fatores de crescimento. Além disso, o KRAS oncogênico coopera com mutações de oncogenes ou genes supressores de tumor para induzir um estroma pró-inflamatório e/ou imunossupressor.
O crosstalk entre KRAS oncogênico, inflamação e mecanismos imunomoduladores no câncer tem como foco principal a ativação do inflamassoma NLRP3 induzida por KRAS e na expressão programada do ligante de PD-1 (PD-L1). O KRAS pode causar escape imune pela via AKT/mTOR via PD-L1. O KRAS suprarregula o PD-L1 através de aumentos na estabilidade do mRNA do PD-L1 por meio da modulação da proteína de ligação ao elemento rico em AU como a tristetraprolina (TTP), mediada pela sinalização MEK a jusante.
Portanto, esses relevantes dados pré-clínicos sugerem que a inflamação induzida por KRAS e sua modulação imune devem definir novas estratégias terapêuticas em ensaios clínicos futuros para a superação dos efeitos induzidos por este oncogene no sistema imunológico. Estudos recentes descreveram o potencial de se combinar inibidores de KRAS G12C com inibidores de checkpoint imunológico, uma vez que esta associação induz à morte de células tumorais (necroptose) e também melhora a sensibilidade do TME aos efeitos da imunoterapia.