 Em mais um tópico da coluna ‘Drops de Genômica’, o oncologista André Murad (foto) discute a função das enzimas PARP e a toxicidade hematológica induzida pelos inibidores de PARP de primeira geração. Confira.
Em mais um tópico da coluna ‘Drops de Genômica’, o oncologista André Murad (foto) discute a função das enzimas PARP e a toxicidade hematológica induzida pelos inibidores de PARP de primeira geração. Confira.
Por André Marcio Murad
O dano ao DNA é um evento comum nas células: aproximadamente 104-105 lesões de DNA celular são experimentadas diariamente em cada uma delas. Em humanos, as proteínas envolvidas na detecção do local da lesão de DNA incluem enzimas da família ADP-ribosiltransferase (PARP1-3/ARTD1-3). No núcleo, as principais enzimas que realizam a poli-ADP-ribosilação são a poli(ADP-ribose) polimerase 1 (PARP1) e PARP2. Essas enzimas se ligam ao DNA danificado e subsequentemente geram cadeias de poli-ADP-ribose (PAR) que atuam como sinais de recrutamento para uma série de fatores de reparo do DNA.
O papel da poli-ADP-ribosilação é estabelecido no reparo de quebra de fita simples (SSBR) e em mecanismos alternativos de junção de extremidades não homólogas (aNHEJ), onde as proteínas-chave envolvidas nas vias de reparo são conhecidas por serem recrutadas para o local de dano ao DNA de uma maneira PAR-dependente. A poli-ADP-ribosilação também inicia a remodelação da cromatina através da ligação de PAR ALC1.
As enzimas PARP1-3 têm uma organização de domínio semelhante na região catalítica C-terminal que consiste em um domínio ADP-ribosiltransferase, um domínio regulador (RD) e um domínio WGR que participa da ligação ao DNA. No entanto, eles diferem em suas partes N-terminais, pois PARP1 contém um domínio BRCA1 C Terminus (BRCT) e três “dedos” de zinco (ZnFs), enquanto os N-terminais de PARP2 e 3 são intrinsecamente desordenados. O domínio WGR de PARP2 demonstrou ser a chave para o reconhecimento de danos no DNA. In vitro, PARP1 pode ser ativada por múltiplas formas de oligonucleotídeos que mimetizam danos no DNA, enquanto PARP2 e PARP3 são especificamente ativadas por quebras de DNA 5'-fosforiladas.
Por outro lado, a eritropoiese é um processo fortemente regulado no qual as células-tronco hematopoiéticas multipotenciais produzem glóbulos vermelhos maduros. Estudos em animais demonstram que a deleção da poli(ADP-ribose) polimerase-2 (PARP-2) em camundongos leva a um quadro de anemia crônica, apesar do aumento dos níveis plasmáticos de eritropoietina, um fenômeno não observado em camundongos sem PARP-1. A perda de PARP-2 causa redução do tempo de vida dos eritrócitos e diferenciação prejudicada dos progenitores eritróides.
Nos eritroblastos, a deficiência de PARP-2 desencadeia estresse replicativo, indicado pela presença de micronúcleos, acúmulo de γ-H2AX (fosfo-histona H2AX) nas células em fase S e fosforilação constitutiva de CHK1 e proteína A de replicação. Estudos adicionais identificam um papel essencial para PARP-2 na eritropoiese, o que justificaria o efeito benéfico que pode surgir do desenvolvimento de inibidores de PARP que inativem especificamente a PARP-1.
Existem quatro inibidores de PARP de primeira geração aprovados em várias indicações de câncer globalmente, e todos eles inibem PARP1 e PARP2. A toxicidade hematológica é um efeito de classe nos inibidores de PARP de primeira geração. A hipótese, portanto, é que um medicamento que tenha como alvo o PARP1 de forma potente e seletiva reduzirá a toxicidade, especialmente a hematológica, melhorará a farmacocinética e a exposição ao alvo e potencialmente melhorará a eficácia, além de permitir opções de combinação mais amplas.
Os inibidores de PARP de segunda geração já estão em fase adiantada de desenvolvimento, projetados como inibidores altamente potentes e seletivos de PARP1 e com atividade de captura de DNA. Não se ligam a nenhum outro membro da família PARP e podem adicionalmente ser também seletivos contra outros alvos oncológicos.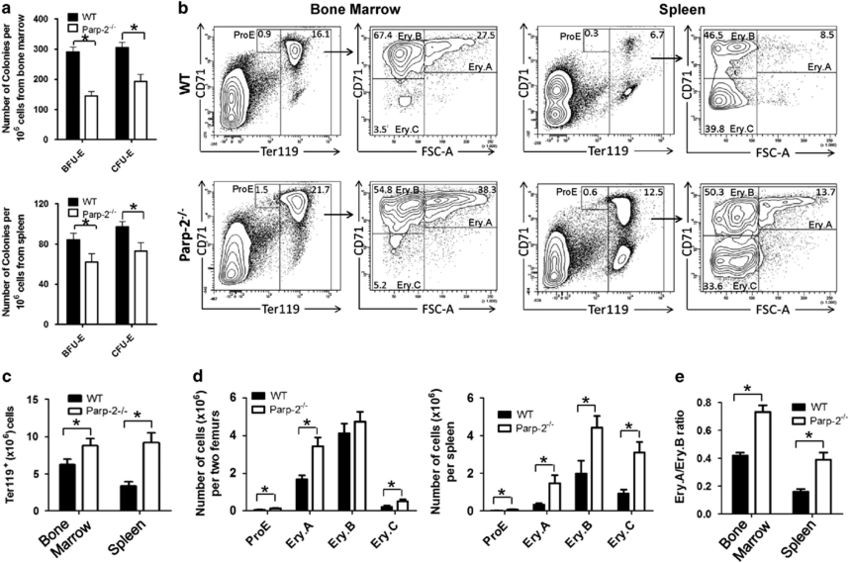
*André Murad é diretor científico do Grupo Brasileiro de Oncologia de Precisão (GBOP), diretor clínico da Personal - Oncologia de Precisão e Personalizada, professor adjunto coordenador da Disciplina de Oncologia da Faculdade de Medicina da UFMG, e oncologista e oncogeneticista da CETTRO Oncologia (DF)




