 A terapia CAR-T Cell axicabtagene ciloleucel (Yescarta®, Kite/Gilead) é aprovada para o tratamento de adultos com linfoma folicular (FL) após ≥2 linhas de tratamento anterior. Na análise de 2 anos do estudo ZUMA-5, as taxas de resposta global em pacientes com linfoma folicular e linfoma de zona marginal tratados com axi-cel foram de 94% (taxa de resposta completa [CR] de 79%) e 83% (taxa de CR de 63%), respectivamente (Neelapu et al. ASH 2021. Abstract 93). Agora, no ASH 2022, Sattva S. Neelapu (foto) e colegas relataram os resultados clínicos e farmacológicos atualizados do estudo após mais de 3 anos de mediana de acompanhamento, demonstrando respostas duráveis contínuas em pacientes com linfoma não-Hodgkin indolente recidivado/refratário, com melhora da sobrevida observada em pacientes com linfoma de zona marginal.
A terapia CAR-T Cell axicabtagene ciloleucel (Yescarta®, Kite/Gilead) é aprovada para o tratamento de adultos com linfoma folicular (FL) após ≥2 linhas de tratamento anterior. Na análise de 2 anos do estudo ZUMA-5, as taxas de resposta global em pacientes com linfoma folicular e linfoma de zona marginal tratados com axi-cel foram de 94% (taxa de resposta completa [CR] de 79%) e 83% (taxa de CR de 63%), respectivamente (Neelapu et al. ASH 2021. Abstract 93). Agora, no ASH 2022, Sattva S. Neelapu (foto) e colegas relataram os resultados clínicos e farmacológicos atualizados do estudo após mais de 3 anos de mediana de acompanhamento, demonstrando respostas duráveis contínuas em pacientes com linfoma não-Hodgkin indolente recidivado/refratário, com melhora da sobrevida observada em pacientes com linfoma de zona marginal.
ZUMA-5 é um estudo de Fase 2, multicêntrico, de braço único de axi-cel em pacientes com linfoma não-Hodgkin indolente (iNHL) recidivado/refratário (R/R) (linfoma folicular e linfoma de zona marginal [MZL]).
Os pacientes elegíveis tinham linfoma folicular recidivado/refratário ou linfoma de zona marginal após ≥2 linhas de terapia (incluindo um mAb anti-CD20 mais um agente alquilante). No momento da inscrição, os pacientes foram submetidos a leucaférese, seguida de quimioterapia condicionante e uma única infusão de axi-cel (2 × 106 células CAR T/kg). O endpoint primário foi a taxa de resposta global (ORR).
Os desfechos de tempo até o evento foram avaliados pelos investigadores em todos os pacientes inscritos. Foram realizadas análises exploratórias de sobrevida linfoma-específica onde as mortes não relacionadas à progressão, axi-cel ou quimioterapia condicionante não foram consideradas eventos de interesse. Análises univariadas e multivariadas foram conduzidas usando análise random forest para classificar a associação de covariáveis farmacológicas com eficácia e toxicidade.
Resultados
Um total de 159 pacientes foram inscritos (127 FL; 31 MZL) e 152 foram tratados com axi-cel (124 FL; 28 MZL). Em 31 de março de 2022, a mediana de acompanhamento dos pacientes inscritos foi de 40,5 meses (intervalo, 8,3-57,4; FL: 41,7, MZL: 31,8). As taxas de ORR e CR foram amplamente semelhantes à análise de 2 anos. Em todos os pacientes inscritos, a mediana de duração da resposta (DOR) foi de 38,6 meses (FL: 38,6, MZL: não atingido [NR]).
A mediana de duração de resposta foi não alcançada em pacientes com resposta completa e foi de 4,9 meses naqueles com resposta parcial. A mediana de sobrevida livre de progressão (SLP) foi de 40,2 meses (FL: 40,2, MZL: NR). A mediana de SLP entre os pacientes com linfoma folicular com (n=70) ou sem (n=41) progressão <2 anos após a quimioimunoterapia inicial (POD24) foi de 40,2 meses e não alcançada, respectivamente.
A SLP estimada de 36 meses foi amplamente consistente em todos os pacientes com iNHL, independentemente de outras características de alto risco, incluindo ≥3 linhas anteriores de terapia e doença duplamente refratária. As medianas de tempo até o próximo tratamento e sobrevida global (SG) não foram alcançadas; a taxa de SG em 36 meses foi de 75%. As medianas de SLP linfoma-específica e sobrevida linfoma-específica não foram alcançadas; As taxas de 36 meses foram de 65% e 89%, respectivamente.
Eventos adversos (EAs) de grau 3 ou superior que ocorreram entre os pacientes tratados desde a análise de 2 anos foram observados, principalmente, em pacientes recentemente inscritos com MZL, incluindo eventos neurológicos em 1, citopenias em 4 e infecções em 2 (1 em linfoma folicular). Desde a análise de 2 anos, 10 pacientes adicionais morreram, 1 devido à progressão, 3 de eventos adversos (nenhum relacionado ao axi-cel) e 6 de outras causas.
Entre os pacientes tratados, os níveis máximos de células CAR T foram maiores naqueles com respostas em andamento em 36 meses (53,9 células/µL) do que aqueles com recidiva (29,6 células/µL) ou não respondedores (22,2 células/µL). Em pacientes com linfoma folicular, os níveis máximos de células CAR T circulantes normalizaram para a carga tumoral basal em conjunto com marcadores inflamatórios pré-infusão elevados e quimiocinas relacionadas às células T reguladoras (Treg) associadas à recidiva. Análises multivariáveis em pacientes com linfoma folicular identificaram ainda mais covariáveis chave que se associam diferencialmente com eficácia e toxicidade.
Em síntese, após 3 anos de acompanhamento no ZUMA-5, axi-cel demonstrou respostas duráveis contínuas em pacientes com linfoma não-Hodgkin indolente recidivado/refratário, com melhora da sobrevida observada em pacientes com linfoma de zona marginal. “Progressão tardia ou morte devido a linfoma ou tratamento em estudo foram incomuns e nenhum novo sinal de segurança surgiu desde a análise de 2 anos. Biomarcadores imunossupressores pré-infusão relacionados a Treg foram associados a recidiva em pacientes com linfoma folicular”, concluíram os autores.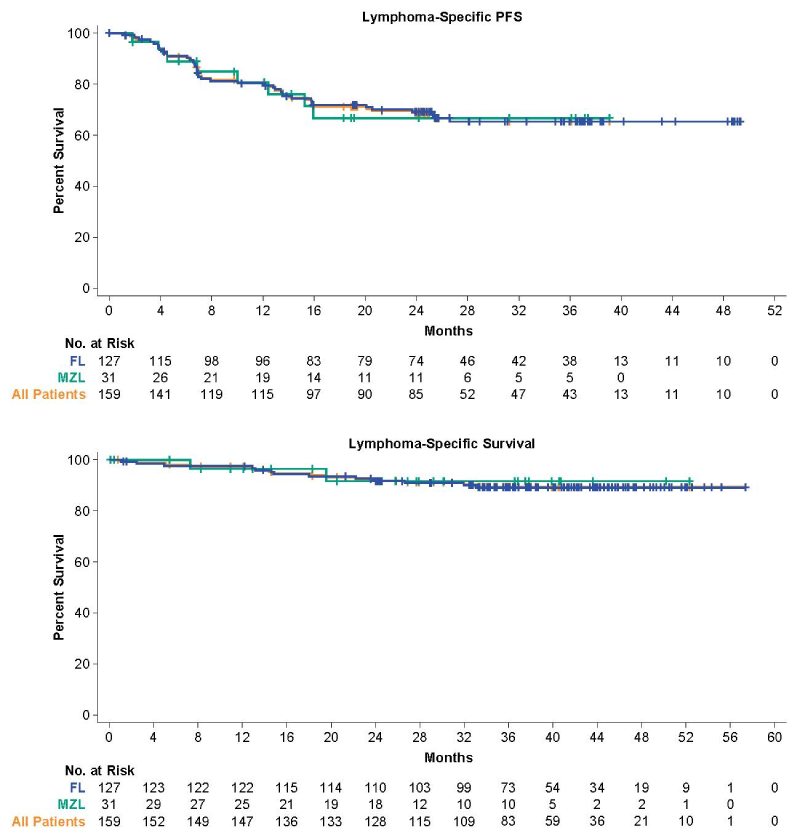
Referência: 4660 3-Year Follow-up Analysis of ZUMA-5: A Phase 2 Study of Axicabtagene Ciloleucel (Axi-Cel) in Patients with Relapsed/Refractory (R/R) Indolent Non-Hodgkin Lymphoma (iNHL)
Program: Oral and Poster Abstracts
Session: 705. Cellular Immunotherapies: Late Phase and Commercially Available Therapies: Poster III
Monday, December 12, 2022, 6:00 PM-8:00 PM
Sattva S. Neelapu, MD et al




