Com seguimento dos pacientes por mais 2 anos desde a primeira apresentação do estudo em 2020, resultados atualizados do ensaio ADAURA apresentados no ESMO 2022 reforçam osimertinibe (Tagrisso®, Astrazeneca) como padrão de tratamento adjuvante para pacientes com câncer de pulmão de células não pequenas (CPCNP) estágio IB-IIIA com mutação EGFR (EGFRm) após ressecção tumoral completa e quimioterapia adjuvante, quando indicada. O seguimento prolongado permitiu a todos os pacientes a oportunidade de completar três anos de tratamento adjuvante e confirmou que osimertinibe manteve benefício sustentado, reduzindo o risco de recorrência da doença ou morte em 77% (razão de risco [HR] de 0,23; intervalo de confiança de 95% [IC] 0,18-0,30) na população da análise primária (Estágios II-IIIA) e em 73% (HR 0,27; IC 95% 0,21-0,34) na população geral (Estágios IB-IIIA).
Na análise primária do estudo de Fase 3 ADAURA (NCT02511106), o benefício favorecendo osimertinibe em relação à sobrevida livre de doença (SLD) foi observado de forma consistente em todos os subgrupos predefinidos, incluindo pacientes com doença estágio IB, II e IIIA que receberam ou não quimioterapia adjuvante. Os dados reportados na New England Journal of Medicine (NEJM, 2020) mostram que a razão de risco (HR) de SLD no CPCNP estágio IIꟷIIIA foi de 0,17; 99,06% CI, 0,11, 0,26; p<0,0001, enquanto em pacientes com doença estágio IBꟷIIIA a razão de risco de SLD foi de 0,20; 99,12% CI 0,14, 0,30; p<0,0001. No ESMO 2022, análises exploratórias atualizadas de sobrevida livre de doença e padrões de recorrência confirmam o benefício após 2 anos de acompanhamento adicional.
Neste estudo randomizado internacional de Fase 3, que contou com a participação de 242 centros de pesquisa, foram inscritos pacientes adultos (idade ≥18 anos; ≥20 Japão/Taiwan) com bom status de desempenho (WHO PS 0/1), com CPCNP EGFRm estágio IBꟷIIIA completamente ressecado (AJCC 7ª edição), tratados com quimioterapia adjuvante, quando indicada. Os pacientes elegíveis foram estratificados pelo perfil mutacional (Ex19del vs L858R) e randomizados 1:1 para osimertinibe 80mg uma vez ao dia ou placebo, por até 3 anos. O endpoint primário foi SLD avaliada pelo investigador no estágio IIꟷIIIA. Endpoints secundários incluíram SLD no estágio IBꟷIIIA, sobrevida global e segurança. Padrões de recorrência e SLD no sistema nervoso central (SNC) foram endpoints exploratórios pré-especificados. O corte de dados foi em 11 de abril de 2022.
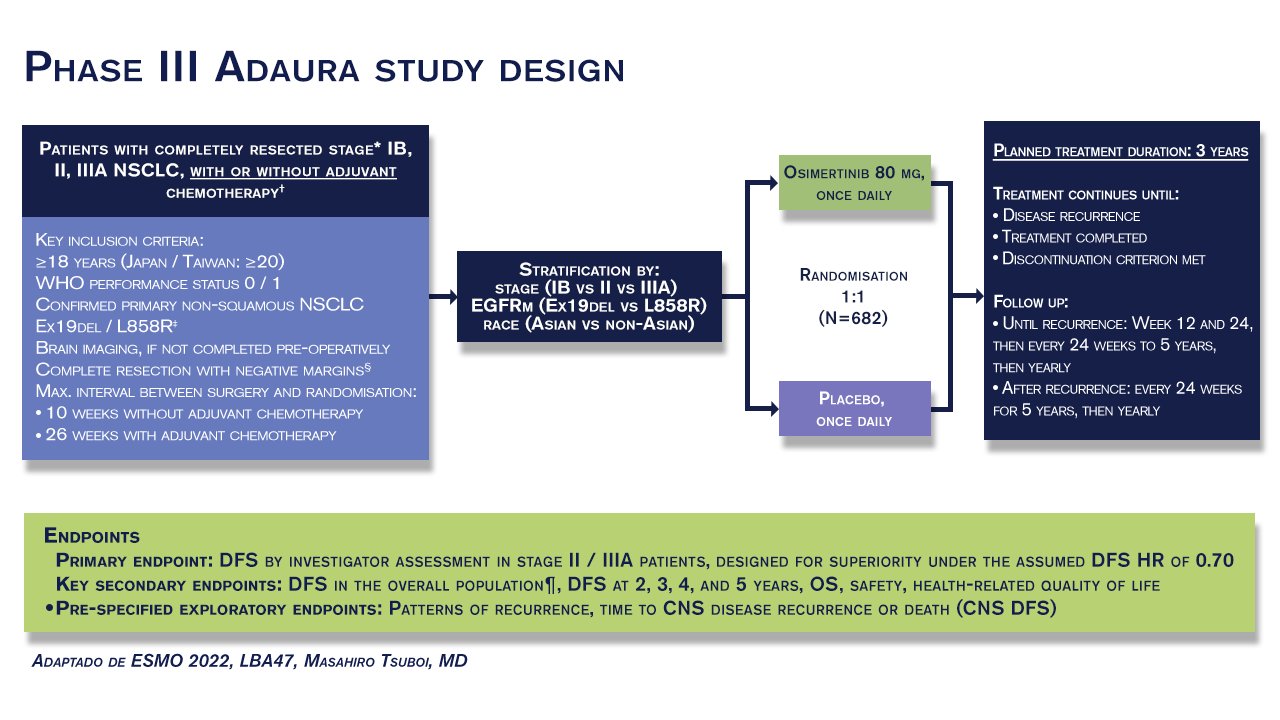
Globalmente, foram analisados 682 pacientes (osimertinibe, n=339; placebo, n=343). Nesta análise atualizada apresentada no ESMO 2022, a taxa de SLD em 3 anos foi de 84% com osimertinibe versus 34% com placebo em pacientes com doença estágio IIꟷIIIA, HR 0,23 (95% CI 0,18, 0,30; 242/470 eventos; 51% de maturidade). Na população geral (estágio IBꟷIIIA), a taxa de SLD em 3 anos foi de 85% com osimertinibe versus 44% com placebo; HR 0,27 (95% CI 0,21, 0,34; 305/682 eventos). Os dados de eficácia mostram mediana de SLD de quase cinco anos e meio (65,8 meses) nas populações primária e geral tratadas com osimertinibe, em comparação com 21,9 e 28,1 meses entre os que receberam placebo.
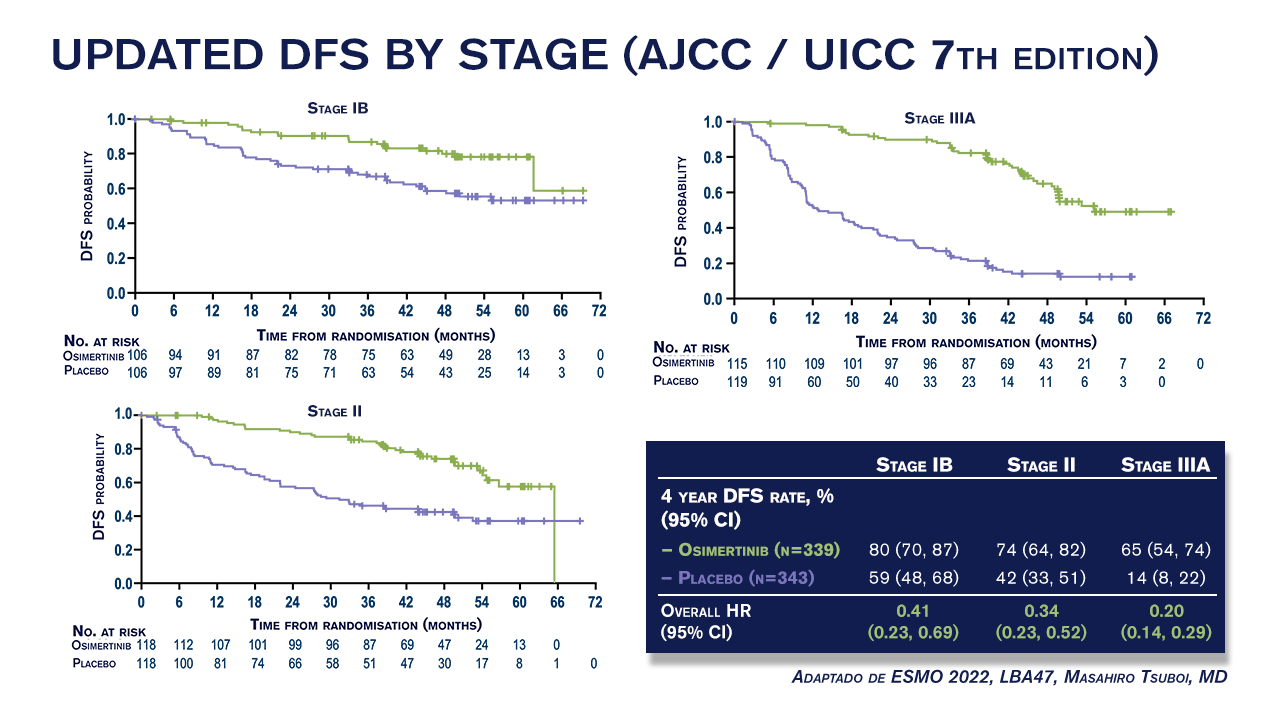
“Um dado bastante interessante apresentado no ESMO 2022 é que o follow up maior, com mais de 2 anos de seguimento, ou seja, com todos os pacientes com possibilidade de receber 3 anos de osimertinibe adjuvante, confirma o benefício importante de osimertinibe adjuvante, com 77% de redução de risco de recorrência ou morte com o uso de osimertinibe versus placebo, um hazard ratio de 0,23 para sobrevida livre de doença em pacientes com doença estádio II a IIIA, que é o desfecho principal. Se consideramos todos os pacientes, a redução de risco é de 73% favorecendo o braço de osimertinibe, com benefício em todos os subgrupos, independentemente do uso da quimioterapia adjuvante”, observa Guiherme Harada, advanced clinical fellow no Memorial Sloan Kettering Cancer Center.
“Quando são analisados os subgrupos, eventualmente se perde o poder estatístico de determinar aquela diferença estatisticamente significativa em cada um deles. Nesse caso, a magnitude de ganho foi tão grande que independente do subgrupo estudado, todos tiveram benefício do uso de osimertinibe, algo que raramente vemos em estudos de Fase 3”, acrescenta Rodrigo Kraft Rovere, oncologista do Hospital Santa Catarina, em Blumenau.
Em síntese, no braço de osimertinibe, menos pacientes experimentaram recorrência local/regional e à distância versus placebo. O tratamento adjuvante com osimertinibe demonstrou benefício significativo na redução do risco de doença no SNC em pacientes com CPCNP estágio II-IIIA (HR: 0,24; 95% CI 0,14-0,42; 63/470 eventos). Aos quatro anos, 90% dos pacientes tratados com osimertinibe estavam livres de doença no cérebro e medula espinhal (IC 95% 85-94%) em comparação com 75% dos pacientes no braço placebo (IC 95% 67-81%).
O perfil de segurança a longo prazo permaneceu consistente com dados já conhecidos de osimertinibe. “A atualização do estudo ADAURA com mais 2 anos de seguimento demonstra que osimertinibe adjuvante continua a prolongar a sobrevida livre de doença nesta população e reduzir a recorrência de doença em sistema nervoso central, um sítio de metástase associado a diversas morbidades que afetam o paciente. Embora dados de sobrevida global ainda sejam aguardados, esses resultados reforçam osimertinibe como terapia adjuvante para pacientes com CPCNP EGFRm estádio IB-IIIA após ressecção cirúrgica”, analisa Harada.
ADAURA é o primeiro estudo global com um inibidor de EGFR a mostrar benefício clínico e estatisticamente significativo no tratamento adjuvante do câncer de pulmão. Diante desses resultados de longo prazo, osimertinibe consolida seu papel no cenário adjuvante do CPCNP em pacientes que abrigam mutação ativadora de EGFR (Ex19del ou L858R), independentemente da exposição à quimioterapia. Mais uma vez, os resultados apresentados por Masahiro Tsuboi, Diretor do Departamento de Cirurgia Torácica e Oncologia do National Cancer Center Hospital, do Japão, e investigador principal do estudo ADAURA, corroboram os benefícios de eficácia e segurança de osimertinibe. “Osimertinibe prolonga notavelmente o tempo que pacientes com câncer de pulmão com mutação de EGFR em estágio inicial estão vivendo livres de câncer após a cirurgia, mas também continua a reduzir o risco de tumores recorrentes no sistema nervoso central ao longo do tempo. Esses resultados reforçam osimertinibe adjuvante como tratamento padrão para esses pacientes”, conclui Tsuboi.
O estudo foi financiado pela AstraZeneca e está registrado em ClinicalTrials.Gov; NCT02511106. https://www.clinicaltrials.gov/ct2/show/NCT02511106
ASSISTA SOBRE O MESMO ASSUNTO:
ADAURA: atualização reforça eficácia de osimertinibe adjuvante no CPCNP estágio IB-IIIA ressecado
Em vídeo, os oncologistas Guilherme Harada e Rodrigo Rovere analisam a atualização do estudo de Fase 3 ADAURA apresentada no ESMO 2022. Os resultados apresentados no encontro europeu confirmam o benefício sustentado de osimertinibe adjuvante no tratamento para pacientes com câncer de pulmão de células não pequenas estágio IB-IIIA com mutação EGFR após ressecção tumoral completa e quimioterapia adjuvante. Assista, na TV ONCONEWS.
Referências:
- Tsuboi, Y. Wu, C. Grohe, T. John, M. Majem Tarruella, J. Wang, T. Kato, J.W. Goldman, S. Kim, C. Yu, H. Vinh Vu, G. Mukhametshina, C. Akewanlop, F. de Marinis, F.A. Shepherd, D. Urban, M. Stachowiak, A.L. Bolanos, X. Huang, R.S. Herbst. Osimertinib as adjuvant therapy in patients (pts) with resected EGFR-mutated (EGFRm) stage IB-IIIA non-small cell lung cancer (NSCLC): Updated results from ADAURA. ESMO Congress 2022, LBA47
- Wu, Y-L., Tsuboi, M., He, J., John, T., Grohe, C., Majem, M., Goldman, J. W., Laktionov, K., Kim, S-W., Kato, T., Vu, H-V., Lu, S., Lee, K-Y., Akewanlop, C., Yu, C-J., de Marinis, F., Bonanno, L., Domine, M., Shepherd, F. A., ... Herbst, R. S. (2020). Osimertinib in resected EGFR-mutated non–small-cell lung cancer: New England Journal of Medicine. New Engl. J. Med., 383(18), 1711-1723. https://doi.org/10.1056/NEJMoa2027071




